|  |
Alla atomer eftersträvar ett fullt yttersta elektronskal. Om ett ämne har fullt i yttersta elektronskalet kallas det att ämnet har ädelgasstruktur. Ädelgaser har redan från början ädelgasstruktur och är därför ovilliga att reagera med andra ämnen.
Bild: Artturi_Mantysaari / Pixabay License
Det finns tre olika strategier för att uppnå ädelgasstruktur: att atomerna delar på elektronerna gemensamt (på två olika sätt) eller att de tar och ger elektroner mellan varandra.
Beroende på atomernas bindning döps den kemiska föreningen olika.
- Metallbindning → metaller
- Molekylbindning → molekyler
- Jonbindning → salter
Till exempel i vatten hålls atomerna ihop med hjälp av en molekylbindning. Alltså är det korrekt att säga vattenmolekyl. Vanligt bordssalt, natriumklorid, är inte en molekyl utan ett salt.
En kemisk förening är ett övergripande ord som innebär att två eller fler grundämnen sitter ihop. Det går inte att kalla rena metaller för kemiska föreningar men många molekyler och alla salter är kemiska föreningar.
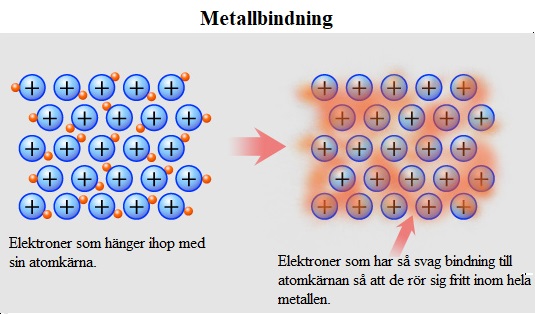
Metallbindningar
Metaller leder elektricitet och värme och därför måste det finnas rörliga laddningar inuti metallen. Dessa rörliga laddningar beror på att varje metallatom släpper ifrån sig sina valenselektroner och har dem gemensamt i ett elektronmoln. Alla metallatomer får då ädelgasstruktur.
Bild: Julen Aduriz EHU / CC BY-SA 4.0
Alla rena metaller har metallbindning och denna bindningstypen är stark. Det krävs generellt höga temperaturer för att få metaller att övergå till flytande form eller till gasform.
Bild: Pavlofox / Pixabay License
Fördjupning:
- Film –What are metallic bonds? (Fuseschool: engelska, 4.13)
- Film – Metallbindningar (Urplay, 2.01, svenska)
- Film – Metallbindningar (Magnus Ehinger, 7.58, svenska)
- Film – How atoms bond (Ted-Ed, 3.34, Engelska)
Uppgifter:
 |  |  |  |  |
Hjälp till att förbättra Ugglans NO! Har du hittat något fel, någon död/olämplig länk eller vill tipsa om någon intressant länk? Skriv en kommentar nedan.