|  |
Redan under forntiden var vissa grundämnen kända. Det var de som kunde hittas i naturen eller som enkelt kunde framställas till exempel guld, silver, koppar, järn och tenn.
Under historiens gång har hela tiden upptäckter av nya grundämnen gjorts, framför allt under 1700-talet och 1800-talet. På mitten av 1800-talet skapade ryssen Dmitrij Mendelejev ett system för hur grundämnena var besläktade med varandra. Detta gjorde han innan atommodellen och protonen var upptäckta.
Bild: geralt / Pixabay License
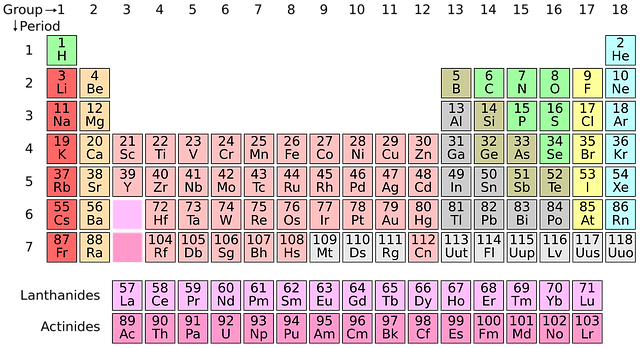
Han kallade sin modell för det periodiska systemet. I hans periodiska system fanns det många tomma rutor för grundämnen som ännu inte upptäckts. Mendelejev kunde, förutom att förutsäga att det fanns oupptäckta grundämnen, även förutsäga dessa grundämnens egenskaper. Idag är de upptäckta och hans förutsägelser stämde.
Det periodiska systemet är indelat i perioder och grupper. En vågrät rad kallas period.
Dessa grundämnen har samma antal elektronskal.
En kolumn (lodrät) kallas grupp. Dessa grundämnen har samma antal valenselektroner d.v.s. lika många elektroner i sitt yttersta skal. Det är endast valenselektronerna som påverkas vid en kemisk reaktion. I en grupp har grundämnena liknande egenskaper (undantag väte). Därför brukar grundämnen i en grupp kallas grundämnesfamiljer.
De flesta grundämnen som finns är metaller (ungefär 95 st). De finns till vänster och i mitten av det periodiska systemet. Ickemetallerna (18 st) finns till höger (undantag väte) och några få halvmetaller (7 st) finns emellan dessa.
Fördjupning:
- Film – Periodiska systemet (Andreas Sandqvist, 6.51, Svenska)
- Film – Grupper och perioder (Magnus Ehinger, 8.23, svenska)
- Hemsida – Periodiska systemet (org)
- Film – The periodic table song(AsapSCIENCE, engelska, 2.53)
- Film – The genius of Mendeleev´s periodic table (TED-ED, engelska, 4.24)
Uppgifter:
 |  |  |  |  |
Hjälp till att förbättra Ugglans NO! Har du hittat något fel, någon död/olämplig länk eller vill tipsa om någon intressant länk? Skriv en kommentar nedan.