|  |  |  |  |
LUFTENS GASER
 |  |
Ovanför våra huvuden finns ett 10 mil högt lager med luftmolekyler. Detta lager, som ligger mellan jordytan och rymden, kallas atmosfär. Atmosfären består av:
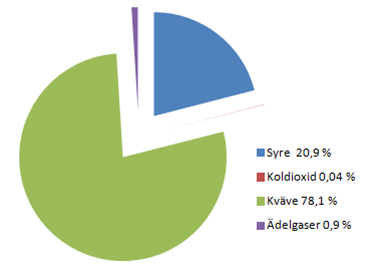
Bild: Oskar Uggla / UgglansNO
Kväve, N2 (78 %)
Atomerna i många gaser sitter ihop två och två till molekyler. Kväve är ett sådant exempel. Kväve är ett grundämne med det kemiska tecknet N.
Kvävgas reagerar inte så lätt med andra ämnen så luften i matförpackningar byts ut till kvävgas vilket gör att maten håller längre. Flytande kväve används för att snabbfrysa mat. Kvävets viktigaste användningsområde är gödseltillverkning.
Syre O2 (21 %)
Syre är ett grundämne som är väldigt reaktivt vilket innebär att det gärna reagerar med andra ämnen. Kemiska föreningar med syre kallas oxider till exempel koldioxid. Som gas i atmosfären sitter syrets atomer ihop två och två.
Syre är ett livsviktigt ämne för organismer. Syret bildas i fotosyntesen som växterna använder för att omvandla solljus till energi. Människor måste andas syre för att kunna leva. Det används för att förbränna maten (cellandning). Syre behövs för att något ska kunna brinna. Det får järn att rosta och koppar att ärga (en form av korrosion)
Ädelgaser He, Ne, Ar, Kr, Xe, Rn (~1%)
Ädelgaserna är sex olika grundämnen. Den vanligaste i luft är argon. Ädelgaser reagerar bara i undantagsfall med andra ämnen. De sitter inte ihop utan finns i luften en och en.
Eftersom ädelgaser ogärna reagerar med andra ämnen finns det många användningsområden för dem. I lampor finns det alltid ädelgas för att lampan ska hålla längre. Helium är en ädelgas som är känd för att ge en rolig röst vid inandning. Helium används också i luftballonger. Neon används för att ge lampors ljus häftiga färger.
Koldioxid CO2 (0,04%)
Koldioxidhalten i atmosfären ökar sakta på grund av förbränningen av fossila bränslen. Koldioxid är en växthusgas. Det innebär att den hjälper till att hålla kvar solens värme i atmosfären istället för att den reflekteras ut.
Koldioxid är livsviktigt för alla organismer eftersom den också är ett ämne som ingår i fotosyntesen och cellandningen.
Koldioxid används för att släcka bränder eftersom ämnet både är tyngre än syre och för att den kväver elden. Då används en kolsyresläckare. Den avger kolsyresnö som är koldioxid i fast form. Anledningen till att koldioxid kväver eld är att eld behöver syre för att brinna och syret trängs bort.
Fördjupning:
- Film – Luft del 1 (Andreas Sandqvist, 5.46, Svenska)
- Film – Luft del 2 (Andreas Sandqvist, 7.17, Svenska)
- Film – Vad är luft? (Studi, svenska, 4.10)
- Film – Syrgas(Studi, svenska, 4.44)
- Film – Kvävgas (Studi, svenska, 4.02)
- Film – Koldioxid och kolmonoxid (Studi, 4.05, Svenska)
- Hemsida – SMHI.se: Luft
- Film – How heavy is air? (Ted-Ed, 3.19, Engelska)
LUFTENS GASER DEL 2
 |  |
Vattenånga
Procenten på beståndsdelarna i luft brukar anges för torr luft vid jordytan.
I atmosfären finns dock även några procent vattenånga. Vattenångan i atmosfären kallas ofta luftfuktighet. Badar du bastu eller befinner dig i regnskog är luftfuktigheten betydligt högre. Är luftfuktigheten 100 % betyder det att luften har tagit upp den maximala mängden vattenånga som det är möjligt. Det går då inte att lösa mer vatten i luften.
Ozon
Halten av ozon i atmosfären är 0,001 procent. Ozon är rent syre. Dessa molekyler består av tre syreatomer, O3. Ozon är giftigt och har en frän lukt. Ozon finns högt upp i atmosfären som ett skydd mot solens energirika UV-ljus. När människor utsätter sig för mycket UV-ljus (till exempel solsemestrar) ökar det risken för hudcancer.
Under 1980-talet upptäcktes stora hål i ozonlagret. De hade skapats på grund av utsläpp av freoner som reagerade med ozonmolekylen. Freoner är en gas som användes i kylskåp. Idag är freoner förbjudna så förstörelsen av ozonlagret har bromsats och ozonlagret håller på att återbildas.
Det finns också en del marknära ozon som bildas när solen skiner på bilavgaser. Det ozonet kan skada växter och djur.
Väte
Väte är universums vanligaste grundämne. Det är huvudbeståndsdelen i universums alla stjärnor. I jordens atmosfär finns nästan inget väte. Det beror på att väte är det lättaste grundämnet av alla. Om väte fanns i atmosfären skulle det stiga och försvinna ut i rymden. Däremot är väte vanligt i kemiska föreningar.
Vatten innehåller väte och allt som lever innehåller stora mängder vatten.
Vätgas innehåller mycket energi så förhoppningsvis kan det användas som bränsle i framtidens bilar. Avgaserna skulle bli vanligt vatten.
Bild: skeeze / Pixabay License
Bilden ovan syns zeppelinaren Hindenburg som råkade ut för en olycka utanför New York och brann upp. Vid tillfället för olyckan var zeppelinaren fylld med väte istället för helium. Hade den varit fylld med helium istället hade förmodligen gasen kvävt elden.
Fördjupning:
- Film – Luft del 3 (Andreas Sandqvist, 9.37, Svenska)
- Film – Luft del 4 (Andreas Sandqvist, 9.12, Svenska)
- Hemsida – Luft (naturvetenskap.org)
- Film – Vätgas (Studi, svenska, 5.03)
- Film – Ozon (Studi, svenska, 4.19)
PÅVISA GASER
 |  |
Inom kemin är det alltid viktigt att kunna påvisa olika ämnen. Att påvisa betyder att ta reda på eller bevisa vilket ämnet är. För att påvisa ett ämne kan en reagens användas. Reagens är ett ämne som reagerar på ett speciellt sätt som bevisar att ett annat ämne finns.
Inom sjukvården används reagenser för att snabbt avgöra om du har för mycket eller för lite av ett ämne i kroppen. Graviditetstest är ett sådant exempel på reagens. Det reagerar med ett speciellt protein som finns i urinen och som det bildas stora mängder av vid graviditeter.
- Syre behövs för att något ska brinna. Om du har något som glöder och för ner föremålet i en bägare med syre kommer en låga att flamma upp.
Bild: Oskar Uggla / UgglansNO
- Koldioxid släcker eld eftersom den tränger undan syret och kväver elden. Koldioxid är tyngre än luft. När koldioxid blandas med kalkvatten bildas ett nytt ämne som gör vattnet grumligt. Koldioxiden i din andedräkt grumlar kalkvatten.
Oskar Uggla / UgglansNO
- Kväve kväver eld likt koldioxid men det grumlar inte kalkvatten och kväve är inte tyngre än syre.
- Om väte blandas med syre och en tändsticka är inblandad blir det en explosion. Blandningen kallas knallgas.
Se filmen Bild: Oskar Uggla / UgglansNO
Fördjupning:
- Film – Syrgas till eld (Petri Matalamaa, svenska, 2.19)
LUFTFÖRORENINGAR
 |  |
Kolmonoxid
När något brinner och det inte finns tillräckligt med syre bildas kolmonoxid. Förbränning med lite syre kallas också för ofullständig förbränning. Kolmonoxid är en mycket giftig gas. När du andas in kolmonoxid tar den syrets plats i blodcellerna och gör att du kvävs vid en hög dos. Rökare har dålig kondition på grund av inandning av kolmonoxid via rökningen.
Nästan varje år dör det människor av kolmonoxidsförgiftning till exempel genom att någon tagit in grillen i huset för att personen fryser. De glödande kolen får inte tillräckligt med syre och får en ofullständig förbränning. Kolmonoxid bildas och kväver människor om det inte finns någon ventilation.
Bild: schottnerballa / Pixabay License
Kolmonoxid kallas också bara koloxid.
Sot
Sot är små partiklar som bildas när fossila bränslen (olja, naturgas, stenkol) förbränns. De kommer till exempel från fabriker och bilavgaser. En partikel är ett föremål som är mikroskopiskt liten till någon millimeter stor. I vissa städer blandas bland annat sot med dimma (vattenångan i luften) och bildar smog.
Bild: Foto-Rabe/Pixabay License
Att vistas i smog är ohälsosamt.
Svaveloxid och kväveoxider
Dessa två gaser kommer från bilarnas avgaser samt från fabrikers utsläpp. De reagerar med vattenångan i luften och faller ner som surt regn. Det innebär att regnet får lågt pH och försurar mark och sjöar. Vid lågt pH kan vissa organismer få svårt att överleva.
Höga partikelhalter
I hårt trafikerade städer kan partikelhalterna i luften bli höga. Partiklarna kommer från att bilarnas bromsar slits och att dubbdäck sliter loss asfalt från vägbanan. På vissa gator i flera städer i Sverige råder det därför dubbdäcksförbud.
Bild: Free-Photos / Pixabay License
Pollen, damm, sand
Partiklar som är tillräckligt små och lätta virvlar runt i luften och ställer till med problem för allergiker och andra med andningsproblem.
Fördjupning:
- Film – time-lapse video shows smog enveloping Beijing (Wall street journal, engelska, 1.26)
- Film – The science of smog (TED-Ed, engelska, 5.43)
- Film – Vad är pollenallergi? (Pollenkoll, svenska, 1.29)
- Film – Air pollution (National geografic, engelska, 3.53)
Uppgifter:
ELD
 |  |
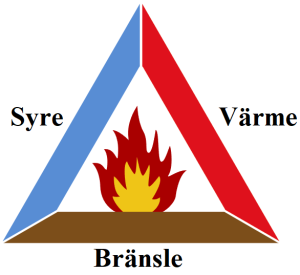
För att bränder ska uppstå krävs det syre, värme och ett brännbart ämne. Ett brännbart ämne är ett ämne som innehåller grundämnet kol.
Bild: Wikipedia/ CC0
Temperaturen ett föremål börjar brinna vid kallas antändningstemperatur eller tändpunkt. Alla ämnen har sin egen antändningstemperatur. Papper börjar till exempel brinna vid 150 grader Celsius.
Innan ett föremål når sin antändningstemperatur brukar det avge brännbara ångor. Den temperatur då ett ämne börjar avge brännbara ångor kallas flampunkt. Till exempel har bensin flampunkten -28 grader Celsius. En del ämnen kan börja brinna av sig självt (självantända) vid rumstemperatur till exempel linolja.
Explosioner är extremt snabba bränder. Vid en explosion bildas mycket gas samt så värms gas i omgivningen upp och tar större plats. Då bildas en tryckvåg. Kraftiga tryckvågor är livsfarliga. De får till exempel hus att rasa.
För att släcka en eld räcker det med att ta bort ett av ”benen” i brandtriangeln. När du släcker en lägereld kan du:
- Hälla på sand – kvävning
- Hälla på vatten – nedkylning
- Sprida ut vedträden – ta bort brännbart ämne
Se klippet Bild: OskarUggla / UgglansNO
I vissa situationer måste du välja metod noga. Ett exempel är när matolja brinner på spisen. Du får aldrig hälla på vatten utan elden måste kvävas. Om du häller vatten på brinnande olja så kommer vattnet att förångas ögonblickligen. När vattnet förångas tar det med sig brinnande droppar av olja. En stor eldkvast skapas.
Fördjupning:
- Film – Eld och brand (Andreas Sandqvist, 7.21, Svenska)
- Film – Aldrig vatten i brinnande olja (Matgeek, svenska, 5.41)
- Hemsida – Eld (org)
- Film – What is fire? (Its okey to be smart, engelska, 4.11)
- Film – What is fire? (Ted-Ed, 4.35, Engelska)
- Film – Begreppa – Eld och brand (ILT inläsningstjänst, Svenska, 3.12)
- Hemsida – Eld – varför brinner det? (skolkemi)
Uppgifter:
METALLER
 |  |
Alla grundämnen delas in i tre grupper: metaller, halvmetaller och ickemetaller.
Majoriteten (80 procent) av alla grundämnen är metaller. Av 118 grundämnen är 17 stycken icke-metaller, 7 stycken halvmetaller och 94 stycken metaller.
Bild: analogicus / Pixabay License
För att räknas som en metall måste följande kriterier uppfyllas:
- Leda elektricitet bra
- Leda värme bra
- Glänsa
- Kunna smidas och gjutas
Några grundämnen kallas halvmetaller. Det innebär att de både har metalliska egenskaper och saknar någon eller några av de metalliska egenskaperna. Exempel på halvmetaller är kisel och arsenik.
BIld: timcgundert / Pixabay License
Ett fåtal metaller finns som ren metall i naturen. De reagerar ogärna med andra ämnen och kallas ädelmetaller. Exempel på ädelmetaller är: guld, silver och platina.
Metaller delas in i grupperna lättmetaller och tungmetaller. Gränsen går vid en densitet på 5kg /dm3. Tabellen nedan visar några exempel.
De flesta metaller finns i marken som kemiska föreningar. Då kallas de mineral. Blandningar av olika mineraler kallas bergart. Om mineralet innehåller värdefulla metaller så det är värt att ta reda på den kallas mineralet för malm.
En blandning av metaller kallas legering. Metaller smälts samman och den nya blandningen får nya, bättre egenskaper.
Viktiga legeringar
Bild: joseph_Berardi / Pixabay License
- Brons (koppar + tenn): Bronset har gett upphov till en hel tidsålder. Brons är en mer hållbar metall än koppar och tenn för sig.
- Stål: (järn + kol): eller rostfritt stål (järn +krom + nickel). Används till bilar, båtar, byggnader m.m.
- Nysilver (koppar + nickel + zink): används till matbestick och smycken.
Bild: Free-Photos / Pixabay License
Fördjupning:
- Film – Andreas Sandqvist: Metaller (youtube, svenska, 9.50)
- Artikel – Wikipedia: aluminium, bly, guld, järn, koppar, platina, silver, tennoch zink.
- Hemsida – Fakta om metaller och mineral (Metalliska material)
- Film – Physical properties of metals and nonmetals (Don´t memorize, engelska, 2.58)
- Film – Chemistry: What is a metal? (Socratica, engelska, 4.27)
Uppgifter:
VATTNETS EGENSKAPER
 |  |
Vatten är ett kemiskt ämne med flera speciella egenskaper. Dessa egenskaper är en av orsakerna till att det finns liv på jorden. Flera av dessa egenskaper beror på vattenmolekylens struktur.
Bild: mariolayaquerevalu / Pixabay License
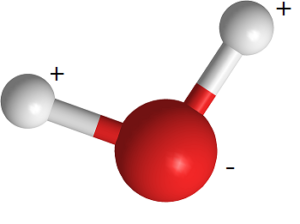
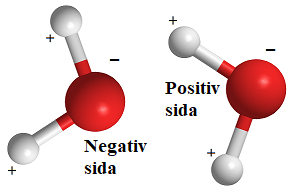
Vattenmolekylens atomer sitter inte i en rät linje utan i en vinkel (se bilden). Den del av vattenmolekylen där syret sitter har en negativ laddning och den sidan med väteatomerna har en positiv laddning. Det innebär att molekylens negativa laddning och de positiva laddningarna inte är på samma ställe. Vattenmolekylen har en negativ och en positiv sida. Det kallas att molekylen är polär.
Vattnets speciella egenskaper:
Bild: mariolayaquerevalu / Pixabay License
Ytspänning
På grund av att vattenmolekylen är polär dras vattenmolekylerna till varandra. En vattenmolekyls positiva del dras till en annans negativa del. Vid ytan på vattnet blir detta extra tydligt. Ytspänningen ger vattnet en seg yta. Ytspänning gör att vissa insekter kan springa på vattenytan och att nålar flyter på ytan.
Kapillärkraft
I ett glas med vatten kan du se att vattnet kryper upp lite längs kanterna. Ifall du varit på sjukhus och lämnat blodprov används smala rör som suger upp blodet automatiskt. Detta beror på att den polära vattenmolekylen påverkas av andra polära molekyler i glasets sida.
Denna egenskap använder växter och träd till att suga upp vatten i sina kärl. Från rötterna ända upp till växterna och trädens toppar.
Lika löser lika
Bild: Oskar Uggla / UgglansNO
Vattnets polära egenskap gör att det endast löser sig med andra vätskor som är polära. Ett talesätt i kemin är att lika löser lika. Om du till exempel blandar vatten med matolja kommer vätskorna att lägga sig i två lager på varandra. Vattenmolekylen är polär medan oljemolekylen inte är det. Dessa två är inte lika och därför löser de sig inte med varandra.
Vattnets densitet
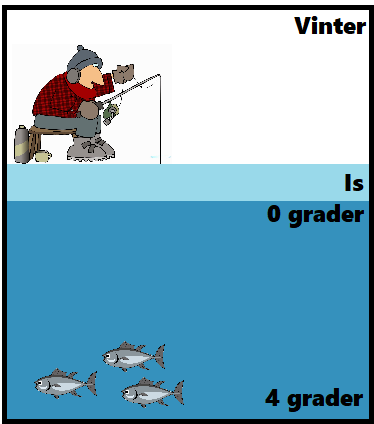
Vatten i fast form, alltså is, har lägre densitet än vatten i flytande form. Det är en väldigt sällsynt egenskap hos kemiska ämnen. På vintern fryser sjöar uppifrån och ner. Isen lägger sig ovanpå vattnet och inte nere vid botten. Detta är en förutsättning för att organismer ska överleva vintern.
Bild: Oskar Uggla / UgglansNO
Vatten har som högst densitet vid fyra grader. Det innebär att när vattnet är fyra grader är det som tyngst och sjunker till botten. I en sjö är det därför alltid fyra grader vid botten. Inte så skön badtemperatur för en människa men helt okej för en fisk.
Värmekapacitet
Bild: Oskar Uggla / UgglansNO
Vatten har hög värmekapacitet. Det innebär att det tar lång tid att värma och kyla vatten. Den bidrar till att temperaturskillnaderna på jorden jämnas ut och att vädret blir stabilare. Denna egenskap gör också att varmt vatten från Golfströmmen värmer upp Norden vilket gör att vi får ett mildare väder. Utan Golfströmmen skulle vi ha ett klimat som på Grönland.
Förmåga att lösa andra ämnen
En lösning är när ett fast ämne är löst i en vätska. Lösta ämnen i vatten syns inte alltid eftersom de är uppdelade i så små delar men ämnena finns ändå där. Tänk dig att du rör ner sockerbit i en kopp te. Sockerbiten syns inte men det smakar sött.
Många olika typer av ämnen kan vara lösta i vatten. Varmt vatten kan lösa mer än kallt vatten. Om det inte går att lösa mer av ett ämne är lösningen mättad.

Bild: Clker-Free-Vector-Images/Pixabay License
I vatten kan det finnas gaser lösta. Det är nödvändigt för fiskarna eftersom de andas syre och inte vattenmolekyler. Kallt vatten löser mer gas än varmt vatten. När kallt vatten värms upp kommer gasen i vattnet att lämna i form av små bubblor.
I kroppen finns det många viktiga lösningar med vatten i huvudrollen till exempel urinen som för ut ämnen kroppen inte behöver. En annan viktig funktion med vatten i huvudrollen är blodet som transporterar runt syre i kroppen. Blodet består till största del av vatten.
Bild: Istock
Många viktiga ämnen till exempel mineraler, är lösta i vatten. Detta är livsviktigt för alla växter som tar upp dessa med sina rötter.
Bild: Pxhere / CC0 Allmängods
Fördjupning:
- Film – Vattnets egenskaper (Andreas Sandqvist, svenska, 7.19)
- Film – Vatten i naturen (Andreas Sandqvist, 3.34, Svenska)
- Film – Vattnets egenskaper (Urplay, 2.16, svenska)
- Film – Ytspänning (Johan Henriksson, svenska, 0.17)
- Film – Why don´t oil and water mix? (Ted-Ed, 5.03, Engelska)
- Film – How polarity makes water behave strangely (Ted-Ed, 3.52, Engelska)
ÖVERSIKT PH
 |  |
Med pH mäts hur surt eller hur basiskt något är. För att kunna mäta pH behöver ämnet vara i en lösning. Det allra vanligast är att mäta pH i ett ämne löst i vatten. Syror är sura och baser är basiska.
- Det som gör något surt är vätejoner, H+. Det är en väteatom som förlorat sin elektron. Ju högre antal vätejoner det är i en vätska desto surare är den. Vätejonen är en del av syran som frigör sig när syran blandas med vatten.
- Det som gör något basiskt är hydroxidjonen, OH–. Det är en molekyl med syre och väte som tagit upp en extra elektron. Hydroxidjonen är en del av basen som frigörs när basen blandas med vatten.
Lösningar som varken är sura eller basiska kallas neutrala. I neutrala lösningar finns inga eller lika många vätejoner och hydroxidjoner
pH-skalan
Bild: OpenStax College / CC 3.0
En pH-skala är en tallinje som sträcker sig från 0 till 14. Extremt sura syror kan ha ett negativt pH-värde.
- Från 0 till 7 är pH-värdet surt.
- Det är neutralt exakt vid pH 7.
- Mellan 7 till 14 är pH-värdet basiskt.
Mellan varje steg på pH-skalan ökar surheten eller det basiska med gånger 10.
- En lösning med pH 2 är 10 gånger surare än en lösning med pH 3.
- En lösning med pH 2 är 100 (10*10) gånger surare än en lösning med pH 4.
- En lösning med pH 2 är 1000 (10*10*10) gånger surare än en lösning med pH 5.
Att ha kunskap om syror, baser och pH är oerhört viktigt eftersom alla organismer påverkas av pH. Organismer överlever endast mellan vissa pH-värden och vid flera miljöproblem är kunskap om pH viktigt. Vid många processer i kroppen är pH-värdet viktigt. Till exempel är blodets pH-värde mellan 7,35 och 7,45 och magsäckens 1,5 – 2,0. Skulle dessa värden förändras och komma i obalans är det livshotande.
Fördjupning:
- Film – Vad är ett pH-värde? (Mona Sohlman, svenska, 3.43)
- Film – What is the pH scale? (Fuseschool, engelska, 3,11)
- Film – pH-scale in simple terms (MooMooMath and science, engelska, 3.08)
- Film – pH in everyday life (Don´t memorize, engelska, 3.49)
INDIKATORER
 |  |
För att mäta pH används indikatorer. Det finns flera olika slags indikatorer.
Universalindikator
Denna indikator är billig att köpa och enkel att använda. Universalindikatorer är preparerade pappersbitar som doppas i lösningar och ändrar färg beroende på lösningens pH. Med den får du ett ganska bra heltalsvärde på pH:t. En universalindikator är en blandning av flera andra olika indikatorer.
BTB
Bild: Oskar Uggla / UgglansNO
BTB är en indikator som är vanlig i skolor. Droppa i några droppar i din lösning så ändrar den färg. BTB är praktiskt för att visa pH-förändring i verkligheten. Sura lösningar ger gul färg, neutrala lösningar ger grön färg och basiska lösningar ger blå färg.
Rödkål
Det finns ett par naturliga indikatorer och rödkål är ett exempel. Droppa i lite saft av kokt rödkål så kommer din lösning ändra färg beroende på pH:t. Rödkål ger ett mer exakt resultat än BTB.
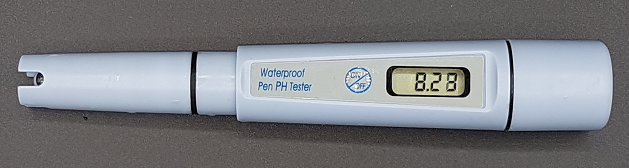
pH-meter
Bild: Oskar Uggla / UgglansNO
En elektrisk apparat som ger ett exakt pH-värde (med en decimal). Detta verktyg används av kemister. pH-metern ger snabba och exakta svar.
Fördjupning:
- Film – Indikatorer och pH (Fredrik Norrström, svenska, 7.11)
- Film – Red cabbage indicator colours (Yucky Science, engelska, 1.49)
- Hemsida – pH-indikator (wikipedia)
- Film – Chemistry indicators (Fuseschool, engelska, 3.09)
- Film – pH indicators explained ( Chem academy, engelska, 7.03)
SYROR
 |  |
En gemensam egenskap för syror är att de fräter. Det betyder att den kan lösa upp andra ämnen. Ju starkare syra desto mer fräter den. Starka syror löser upp många metaller och bildar bland annat vätgas. En blandning av saltsyra och salpetersyra kallas kungsvatten och kan även lösa upp ädelmetallen guld. Syror finns ofta i livsmedel.
Det som avgör styrkan på syran är två saker.
1) Hur koncentrerad den är. Det betyder hur mycket vatten den är utspädd med.
2) Om det är en stark eller svag syra. Starka syror släpper ut alla sina vätejoner från syramolekylen medan svaga syror bara släpper ut en del av dem.
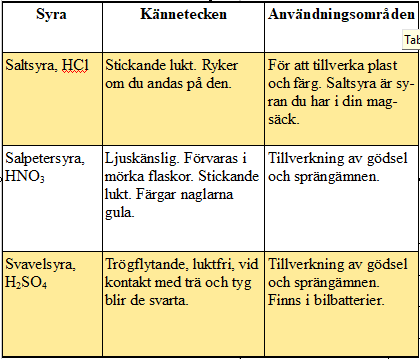
De tre vanligaste starka syrorna:
Dessa tre syror är vanliga i skolan och är väldigt farliga. Var försiktig när du använder dem. Ska du späda syran så glöm inte SIV-regeln. Häll Syran I Vattnet.
Några svaga syror:
I naturen finns många svaga syror. Naturliga syror kallas växtsyror eller organiska syror.
- Citronsyra finns naturligt i citrusfrukter. Den används även flitigt i livsmedel för att de inte ska härskna eller ändra färg.
- Kolsyra är en svag syra som finns i läsk. Det som bubblar i läsken är att kolsyremolekylen faller sönder och avger koldioxid.
- Mjölksyra bildas i musklerna vid hård träning. Det beror på att musklerna inte får tillräckligt med syre. Mjölksyra bildas i mjölk när den surnar.
- Ättikssyra används mycket i matlagning (utspädd). Den förbättrar smaken och gör maten mer hållbar.
- Myrsyra är försvarsvapen hos myror och det som bränns i brännässlor. Det används för att konservera gräs åt kossorna (ensilage).
Fördjupning:
- Film – Syror (Andreas Sandqvist, 9.31, Svenska)
- Film – Syror och baser del 1 (brom8305, svenska, 10.01)
- Film – Kemi 6 syror och baser (Eva-Karin Wiklund, svenska, 22.57)
- Film – Syror (Urplay, 2.16, svenska)
BASER NEUTRALISATION
 |  |
Baser är inte lika vanligt förekommande som syror varken i naturen eller i livsmedel. Baser kan lösa upp fetter och vissa proteiner så därför är rengöringsmedel ofta basiska till exempel tvål, tvättmedel och maskindiskmedel. Baser känns lite hala om du har lite mellan fingrarna.
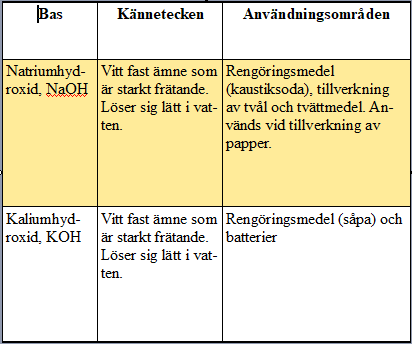
Starka baser:
Svaga baser:
Neutralisation:
Blandas en syra med en bas kommer vätejonen och hydroxidjonen att reagera med varandra och bilda vatten. En farlig syra kan blandas med en farlig bas och resultatet blir en ofarlig neutral lösning.
Syra + Bas → Vatten + Salt
HCl + NaOH → H20 +NaCl (koksalt)
Denna kunskap har sedan 70-talet använts för att höja pH-värdet i försurade sjöar.
Ett miljöproblem är utsläpp av svaveloxider och kväveoxider från industrier och fordon. Dessa ämnen i kontakt med vattenånga reagerat, blivit svavelsyra och salpetersyra och sedan fallit ner på jorden som surt regn. Surt regn har lett till att vattendrag fått ett lägre pH-värde och att växt- och djurliv därför haft svårare att överleva.
För att komma till rätta med detta släpps kalk ner i sjöar för att neutralisera det sura. Sedan åtgärden inleddes på 1970-talet har kalkningen av sjöar minskat eftersom de utsläpp, som leder till surt regn, minskat mycket.

Fördjupning:
- Film – Baser (Andreas Sandqvist, 5.28, Svenska)
- Film – Syror och baser del 2 (brom8305, svenska, 13.00)
- Film – Baser (Urplay, 1.44, svenska)
- Film – The strengths and weaknesses of acids and bases (Ted-ed, engelska, 3.47)
RENA DRICKSVATTEN
 |  |
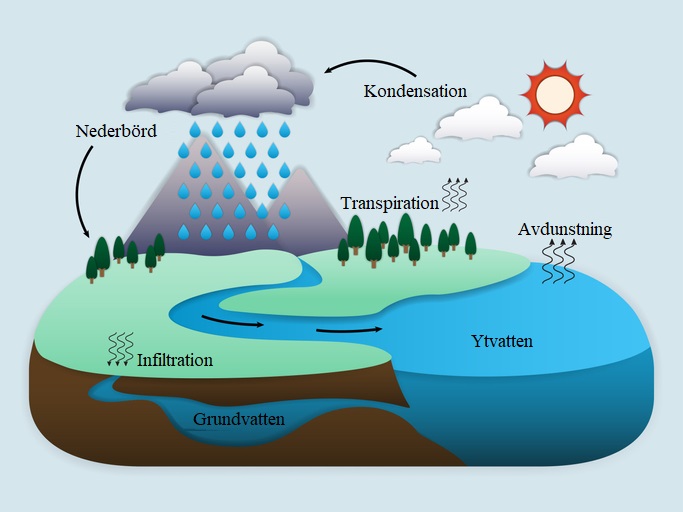
Allt liv innehåller vatten och rent vatten är nödvändigt för alla organismer. Nästan allt vatten på jorden är saltvatten (97 %). En stor del av sötvattnet (2 %) är bundet till jordens glaciärer. Det vatten som finns tillgängligt för oss människor (1 %) att använda finns långt ner i marken som grundvatten eller i sjöar och vattendrag som ytvatten.
Bild: Istock
Tillgången till vatten är väldigt olika i världen. I Europa och framför allt Norden finns det gott om vatten. I vissa delar av Afrika, Asien och i Mellanöstern är det ständig brist på vatten. Vattenbristen gör ibland att skördar torkar bort vilket leder till matbrist.
I länder med stor vattentillgång förbrukas också mycket mer vatten. En person i Sverige förbrukar ungefär 180 liter vatten om dagen. 6000 liter förbrukas om även virtuellt vatten räknas med. Virtuellt vatten är vatten som man inte direkt använder utan som behövs för att tillverka livsmedel samt de prylar och kläder människor använder.
Foto: Btw water / med tillstånd
Vattenrening: dricksvatten
För att vattnet inte ska ta slut måste det återvinnas. Innan det återvinns måste det renas. Grundvattnet kommer bland annat från regn som sakta filtreras i håligheter nere i marken. Det filtrerade grundvattnet är så rent att det kan användas utan några åtgärder. Ytvattnet från sjöar och vattendrag behöver genomgå olika processer innan det går att dricka.
Så här går det till i ett reningsverk:
- Grovfiltrering – Stora föremål tas bort ur vattnet till exempel löv, grenar, sjögräs, skräp och slam.
- Kemisk rening – För att få bort små partiklar av lera och smuts i vattnet tillsätts flockningsmedel i vattnet. Det gör att smutsen klumpar ihop sig. Processen kallas flockning. Smutsen sjunker till botten (sedimenteras) och kan därefter tas bort.
- Filtrering – Vattnet rinner genom sand som tar bort de sista partiklarna.
- pH-justering – Om det behövs regleras pH-värdet. pH måste ligga mellan 6 och 9.
- Desinfektion – Detta sista steg innebär att de bakterier som kan finnas i vattnet dödas. Det sker med klor, ozon eller med UV-ljus. Ibland kan vattnet behöva luftas för att få bort illaluktande gaser.
- Nu går vattnet att dricka. Vanligtvis pumpas vattnet till ett vattentorn där det förvaras i väntan på att användas.
Fördjupning:
- Film – Vatten i vardagen och samhället (Andreas Sandqvist, 9.10, Svenska)
- Film – Lär dig mer om vattenbrist (Therese Zätterqvist, svenska, 6.03)
- Film – Vatten och vattnets egenskaper (Fröken Ulle, svenska, 6.38)
- Hemsida – Produktion av dricksvatten (svensktvatten.se)
- Hemsida – Reningsprocesser i vattenverk (svensktvatten.se)
- Film – Ditt viktigaste livsmedel (Norrvatten)
- Film – Vattenverk (Explainer.se, svenska, 2.29)
- Film – Vattenrening (Urplay, 5.30, svenska)
- Film – Färskvattenbrist: En introduction till problemet (Ted-Ed, 3.39, Engelska)
- Film – Where we get our fresh water (Ted-Ed, 3.47, Engelska)
- Film – Are we running out of clean water? (Ted-Ed, 5.19, Engelska)
- Film – What is groundwater? (GRS, 4.04, engelska)
Uppgifter:
RENA AVLOPPSVATTEN
 |  |
Bildkälla: Istock
Vattnet som vi använder rinner ut i avloppet och det måste naturligtvis renas innan det släpps tillbaka till naturen. Reningen sker i fyra steg:
Mekanisk rening – Här tas fasta föremål bort från vattnet till exempel papper, plast och andra saker som inte borde ha spolats ner i toaletten.
Biologisk rening – Med hjälp av mikroorganismer till exempel bakterier bryts biologiskt material ner (matrester och bajs) till koldioxid och vatten. En del material tas tillvara på och används för att tillverka biogas.
Kemisk rening – Kemiska ämnen (flockningsmedel) blandas i främst för reagera med fosfor i vattnet. De kemiska föreningar som bildas sjunker till botten och kan tas bort. Processen kallas flockning. Om stora mängder fosfor kommer ut i naturen orsakar det övergödning.
Kväverening – Detta steg finns inte i alla reningsverk eftersom det kan lösas på naturligt sätt. Poängen med detta steg är att omvandla kväveföreningar till kvävgas.
Bildkälla: Pixelbay
Efter dessa steg släpps vattnet ut i ett närliggande vattendrag igen. Anledningarna till att det är viktigt att rena vattnet är:
- Det förhindrar att vattenburna sjukdomar sprids.
- Det minskar övergödning och bottendöd.
- Det förhindrar förgiftning från miljögifter och läkemedelsrester.
I en toalett får man endast spola ner toalettpapper och saker som passerat genom kroppen t.ex.avföring.
Föremålen nedan får man inte spola ner.

Fördjupning:
- Film – Vatten i vardagen och samhället (Andreas Sandqvist, 9.10, Svenska)
- Film – Lär dig mer om vattenbrist (Therese Zätterqvist, svenska, 6.03)
- Film – Vatten och vattnets egenskaper (Fröken Ulle, svenska, 6.38)
- Hemsida – Produktion av dricksvatten (svensktvatten.se)
- Hemsida – Reningsprocesser i vattenverk (svensktvatten.se)
- Film – Ditt viktigaste livsmedel (Norrvatten)
- Film – Vattenverk (Explainer.se, svenska, 2.29)
- Film – Vattenrening (Urplay, 5.30, svenska)
- Film – Färskvattenbrist: En introduction till problemet (Ted-Ed, 3.39, Engelska)
- Film – Where we get our fresh water (Ted-Ed, 3.47, Engelska)
- Film – Are we running out of clean water? (Ted-Ed, 5.19, Engelska)
- Film – What is groundwater? (GRS, 4.04, engelska)
 |  |  |  |  |